Análisis del memorando de política científica regulatoria de la FDA: los productos de verificación de edad reciben una revisión prioritaria, los sabores distintos del tabaco deben demostrar un beneficio incremental
Dejar un mensaje
Análisis del memorando de política científica regulatoria de la FDA: los productos de verificación de edad reciben revisión prioritaria, los sabores distintos del tabaco deben demostrar un "beneficio incremental"

El 21 de noviembre, la FDA emitió 13 memorandos de políticas científicas sobre la revisión del PMTA. 2Firsts se comunicó con varios expertos en cumplimiento y descubrió que los productos de cigarrillos electrónicos con "tecnología de verificación de edad" se revisarán primero; Al mismo tiempo, la FDA reveló que los cigarrillos electrónicos sin sabor a tabaco deben demostrar "beneficios incrementales" para los fumadores adultos, y las aplicaciones que no proporcionan ensayos controlados aleatorios o datos de investigación a largo plazo pueden considerarse "defectos fatales".
El 21 de noviembre, la Administración de Alimentos y Medicamentos de EE. UU. (FDA) emitió 13 memorandos sobre política científica para la revisión de las solicitudes previas a la comercialización de cigarrillos electrónicos, que abarcan de 2020 a 2023. La FDA dijo que estos memorandos describen el proceso y los métodos prioritarios utilizados para presentar y revisar los cigarrillos electrónicos con sabor y otros PMTA (detalles: la FDA de EE. UU. emite 13 memorandos de política científica regulatoria: enfoque en los métodos de revisión de los cigarrillos electrónicos con sabor).

La FDA publica un memorando de política científica regulatoria relacionada con el PMTA|Fuente: FDA
Con respecto al contenido del memorando publicado esta vez, 2Firsts consultó materiales relevantes y se comunicó con muchos expertos en cumplimiento y descubrió que la importancia de la "tecnología de verificación de edad" estaba claramente establecida, es decir, los dispositivos con verificación de edad recibirán una revisión prioritaria. Al mismo tiempo, algunos memorandos también revelaron los detalles de los requisitos adicionales de la FDA para la investigación de sabores en revisiones posteriores.
Los productos con verificación de edad pueden recibir revisión prioritaria
Un memorando titulado "Priorización de presentación de PMTA recibidas entre el 10 de septiembre de 2020 y el 3 de noviembre de 2021" detalla la política y los antecedentes de la FDA para priorizar las solicitudes de productos de tabaco previas a la comercialización (PMTA) recibidas.

Priorización de presentación de PMTA recibidas entre el 10 de septiembre de 2020 y el 3 de noviembre de 2021 Memorando|Fuente: FDA
En el memorando, la FDA explicó los principios básicos de sus prioridades de revisión, que incluyen principalmente los dos aspectos siguientes:
Según la fecha de presentación: los PMTA generalmente se revisan en el orden de las fechas de presentación. Por ejemplo, los productos enviados el 10 de septiembre tendrán prioridad sobre las solicitudes enviadas el 15 de septiembre.
Prioridades especiales: se pueden priorizar algunas aplicaciones con tecnologías especiales o importancia para la salud pública. Por ejemplo, el memorando mencionaba específicamente que una empresa presentó un PMTA con "tecnología de selección de edad", a la que se le dio prioridad debido a su posible impacto en la salud pública. La FDA declaró que "se dio prioridad a la presentación de la solicitud porque contiene una supuesta tecnología de control de edad".

"La aplicación fue priorizada porque contiene la supuesta tecnología de verificación de edad|Fuente: FDA
"El memorando muestra el hecho de que los productos con "verificación de edad" pueden revisarse más rápidamente y pasar la segunda ronda de revisión, pasando directamente a la tercera etapa de revisión". dijo Kurt, consultor experto en cumplimiento de 2Firsts.
Kurt dijo: "Tengo entendido que la FDA dará prioridad a la revisión de los productos de verificación de edad y acelerará directamente la cola a la tercera etapa de revisión, pero los estándares de revisión no se han reducido".
También cree que la lógica de revisión de la FDA sobre los cigarrillos electrónicos se puede ver en esto: los dispositivos con funciones de verificación de edad pueden evitar eficazmente que los adolescentes los utilicen, por lo que se consideran una prioridad.
Dijo que es posible que tales productos no necesiten someterse a costosos ensayos controlados aleatorios (ECA) o estudios de cohortes a largo plazo (estudios de cohortes longitudinales), porque sus dispositivos terminales ya han desempeñado un papel preventivo en el abuso de adolescentes.
Los productos aromatizantes deben demostrar "beneficios incrementales"
En otro memorando titulado "ENDS que contienen líquido electrónico sin sabor a tabaco: enfoque para los PMTA1 que no se encuentran en revisión científica sustancial (Fase III)", la FDA analizó la estrategia de gestión de la aplicación previa a la comercialización de productos de tabaco (PMTA) para e-líquidos sin sabor a tabaco. -cigarrillos (TERMINA).
En el memorando, la FDA explicó sus propios estándares de revisión. La agencia citó la Sección 910 de la Ley Federal de Alimentos, Medicamentos y Cosméticos de EE. UU. (Ley FD&C). La clave de la revisión es si el producto es adecuado para "proteger la salud pública" (APPH). Los cigarrillos electrónicos sin sabor a tabaco deben demostrar que tienen "beneficios incrementales" (beneficios incrementales) para los fumadores adultos en comparación con los productos con sabor a tabaco. beneficio).
El "beneficio incremental" puede entenderse como que la FDA exige que los remitentes de cigarrillos electrónicos sin sabor a tabaco demuestren que brindan beneficios adicionales a los fumadores adultos en comparación con los productos con sabor a tabaco u otras opciones existentes, y la evaluación requiere evidencia de ensayos controlados aleatorios (RCT). ) o estudios de cohortes a largo plazo.
Si la solicitud carece de la investigación anterior, se considerará un "defecto fatal" y puede resultar en una orden de denegación de comercialización (MDO).

Descripción del "defecto fatal"|Fuente: FDA

Descripción del "defecto fatal"|Fuente: FDA
Kurt dijo que desde julio de 2021, la FDA ha agregado requisitos de pruebas clínicas a largo plazo para sabores al proceso de revisión. Este requisito adicional ha provocado que un gran número de empresas sean consideradas no calificadas y se hayan emitido miles de órdenes de rechazo del mercado a empresas. Posteriormente, estas empresas han presentado múltiples demandas contra la FDA, argumentando que este requisito adicional viola los estándares de revisión originales de la PMTA.
Entonces, ¿cómo define la FDA los "sabores que no son de tabaco"?
Un memorando titulado "Apéndice al enfoque de los PMTA1 para ENDS2 sin sabor a tabaco que no se encuentran en revisión científica sustantiva (Fase III)" proporciona una respuesta. La FDA enumera claramente qué productos pertenecen a sabores distintos del tabaco en este submemorándum y define el alcance de los sabores "tabaco" y "menta".
Kurt dijo que los sabores de tabaco y mentolados en estas dos listas no se revisarán como productos de sabor. Solo FLAVOR SKU estará sujeto a revisión de ensayos clínicos a largo plazo con defectos fatales. Si no hay evidencia relevante, la FDA les enviará una carta MDO.
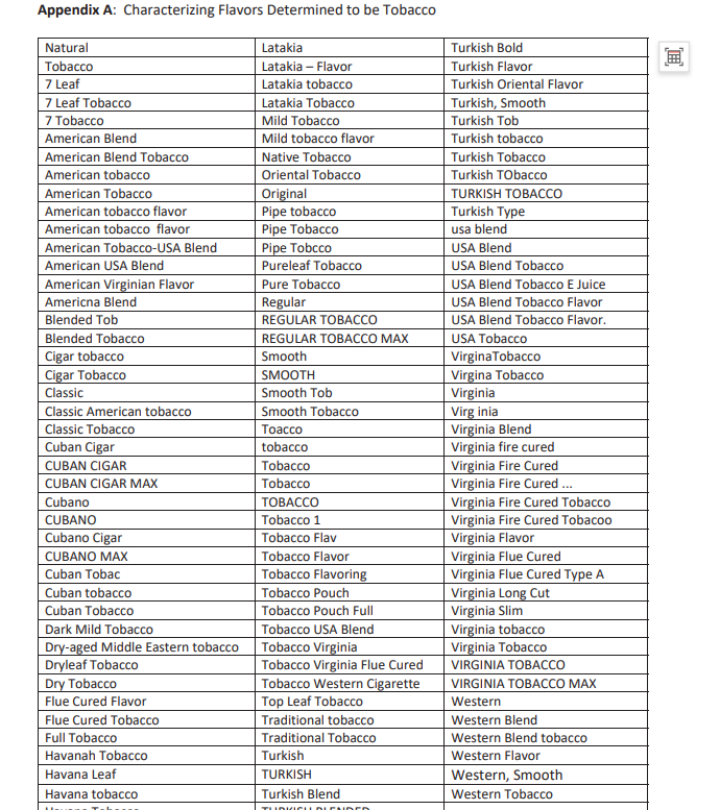
Lista de memorandos sobre cigarrillos electrónicos con sabor a tabaco que no han sido objeto de una revisión científica sustancial|Fuente: FDA

Lista de memorandos sobre cigarrillos electrónicos con sabor a tabaco que no han sido objeto de una revisión científica sustancial|Fuente: FDA

Lista adjunta de memorandos sobre cigarrillos electrónicos con sabor a tabaco que no han sido objeto de una revisión científica sustancial|Fuente: FDA
Este es el cuarto lote de memorandos emitidos en 2024, y la FDA ha emitido un total de 26 memorandos de política científica regulatoria. Aunque la FDA declaró que los memorandos publicados no deben usarse como herramientas, pautas o manuales para preparar solicitudes o enviar documentos a la FDA. Sin embargo, el análisis y la interpretación de estos memorandos aún ayudan a tener una comprensión más profunda y precisa de la filosofía y los métodos de la FDA para la revisión de los cigarrillos electrónicos.
Los dos supremos seguirán prestando atención a los últimos avances en la política regulatoria de los cigarrillos electrónicos de EE. UU.









